Titel: Botanik: Ein seltener Fund - Ceratozamia robusta *
Beitrag von: Fahrenheit in März 08, 2019, 16:36:14 NACHMITTAGS
Beitrag von: Fahrenheit in März 08, 2019, 16:36:14 NACHMITTAGS
Liebe Pflanzenfreunde,
wo gefunden? Im seit Juni des vergangenen Jahres geöffneten neuen Gewächshaus des Botanischen Gartens Bonn, das im Mittelbeet auch die einzige Sansevieria sambiranensis (jetzt Dracaena sambiranensis) in einem deutschen Botanischen Garten beherbergt. Die Pflanze ist umgeben von einigen schönen Palmfarnen und ich hatte die Tage die Chance, von einem Gärtner ein abgeknicktes Fiederblatt von Ceratozamia robusta zu erhalten.
Ceratozamia ist mit 28 hauptsächlich in den Gebirgszügen Mittelamerikas vorkommenden Arten eine eher kleine Gattung in der Ordnung der Cycadales und die Probe erlaubt mir den Blick auf die Blattanatomie einer weiteren Gattung.
Bild 1: Kladogramm der Ordnung Cycadales mit den bereits von mir beprobten Gattungen
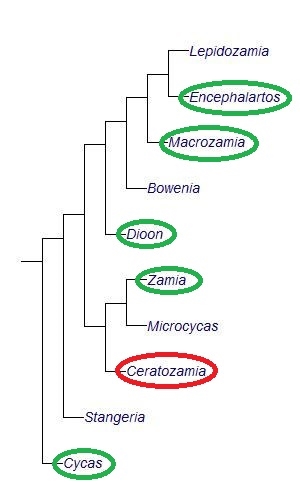
Einen Überblick über meine Beiträge zu den Cycadales findet Ihr hier zu Beginn des Artikels: https://www.mikroskopie-forum.de/index.php?topic=29879.0
Nach nun fast drei Jahren also wieder einmal ein neuer Palmfarn!
Wie immer zunächst etwas zur Pflanze selbst
Ceratozamia robusta ist - obwohl die größte Art der Gattung - ein mittelgroßer Palmfarn, dessen Vorkommen sich von Belize über Guatemala bis nach Mexiko (Oaxaca, Veracruz und ggf. Chiapas) erstreckt. Er findet sein Habitat im Unterholz feuchter, sumpfiger Regenwälder. Die Erstbeschreibung erfolgte 1847 anhand von im Europa kultivierter Pflanzen mit nicht näher bestimmtem Ursprung in Mexiko. Daher wurde 1986 ein Neotyp anhand von Proben verschiedener Pflanze aus Chiapas festgelegt.
Bild 2: Die Pflanze im Botanischen Garten Bonn mit 7 Blättern

Der Oberirdischer Stamm von Ceratozamia robusta erreicht eine Höhe von bis zu 2 m mit einem Durchmesser von ca. 30 cm. Der Stamm ist gelegentlich an der Basis verzweigt. Wie bei den Cycadales üblich ist er von den Blattbasen abgestorbener Blätter bedeckt.
Bild 3: Stamm der bonner Pflanze

Der kleine, kugelige Stamm weist auf ein junges Exemplar hin. An der rechten Seite ein junger Wedel von einem Nebenstamm - ein Hinweis auf die vegetative Vermehrung der Pflanze
Die junge Blätter sind blassgrün und unbehaart. Die Pflanze trägt 8 bis 30 ausgewachsene Blätter, die oft in einer dichten Krone angeordnet sind. Jedes Blatt ist 1,5 bis 3 Meter lang, dunkelgrün und ebenfalls unbehaart. Die einzelnen Blätter oder Wedel haben eine grade bis leicht gebogene Form. Der an der Basis wollig behaarte Blattstiel ist 20 bis 60 cm lang und mit vielen kleinen Stacheln besetzt. Die Rhachis ist gerade bis leicht spiralig gebogen. Pro Blatt finden sich 100 bis 200 lanzettförmige und parallelnervige Fiederblätter mit umgebogenem glatten Rand und spitzem Apex.
Bild 4: Junge Plfanze

Wikipedia, User C. T. Johansson, CC BY-SA 4.0
Der männliche Zapfen ist ca. 30-50 * 10 - 14 cm groß, zylindrisch und steht aufrecht. Die gelblichgrünen Mikrosporophylle tragen 2 kleine, hellbraune Hörnern. Der Fruchtstandsstiel (Peduncle) ist bei einer Dicke von 2,5 cm gut 10 cm lang und auch wollig behaart.
Bild 5: Männliche Zapfen

Wikipedia, User C. T. Johansson, CC BY-SA 4.0
Bild 6: Etwas näher heran erkennt man die beiden Hörnchen an den Enden der Mikrosporophyllen

Crop aus Bild 5, Wikipedia, User C. T. Johansson, CC BY-SA 4.0
Der weiblicher Zapfen erreicht eine Größe von 30 - 50 * 10 - 14 cm, ist ebenfalls zylindrisch geformt und steht aufrecht auf dem etwa 15 cm langen und 2,8 cm dicken Peduncle. Er ist grüngrau gefärbt und die Makrosporophyllen tragen je zwei gut ausgebildeten, kräftigen Hörnern, die farblich nicht abgesetzt sind. Der eiförmige Samen mit weißer Sacrotesta ist etwa 2,5 * 2 cm groß und glatt.
Bild 7: weiblicher Zapfen

Cycads of the World, David L. Jones, S. 121
Beschreibung übertragen aus Cycads of the World von David L. Jones, Smithsonian, zweite Auflage 2002.
Wie immer die Informationen zur Präparation
Probenahme im Botanischen Garten Bonn: ich habe von einem Gärtner ein abgeknicktes Fiederblatt erhalten.
Geschnitten habe ich auf dem Tempelchen (Zylindermikrotom im Halter als Tischmikrotom) mit Leica Einmalklingen 818 im SHK Halter. Das Blatt ist sehr zäh und ließ sich in Möhreneinbettung nicht ganz so gut schneiden (Schnittdicke ca. 50µm).
Anschließend erfolgte die Schnittfixierung in AFE für ca. 14 Stunden. Nach stufenweiser Überführung in Aqua dest stand eine rund dreiminütige Behandlung mit Eau de Javel (DM, Reinigungsprodukt in der Literflasche für kleines Geld mit 2,6g NaClo auf 100 ml) an. Danach habe ich wieder sehr gründlich mit Aqua dest. gespült, bis kein Chlorgeruch mehr erkennbar war. Den Abschluss der Vorbereitungen bildete die Bleiche mit Chloralhydrat (160g auf 100 ml Aqua dest.) für ca. 12 Stunden. Nach einem weiteren sehr gründlichen "Spülgang" waren die schnitte dann bereit für die Färbung.
Gefärbt habe ich nach Überführen in Aqua dest. mit W3Asim I nach Rolf-Dieter Müller für ca. 8 Minuten mit einmaligen Erwärmen bis kurz vor den Siedepunkt.
Eingedeckt wurden die Schnitte nach gründlichem Entwässern mit reinem Isopropanol wie immer in Euparal.
Kurz zur verwendeten Technik
Die Aufnahmen sind auf dem Leica DMLS mit den PlanApos 10x, 20x, 40x und 100x (öl) entstanden. Die Kamera ist eine Panasonic GX7, die am Trinotubus des Mikroskops ohne Zwischenoptik direkt adaptiert ist. Die Steuerung der Kamera erfolgt durch einen elektronischen Fernauslöser. Die notwendigen Einstellungen zur Verschlusszeit und den Weißabgleich führe ich vor den Aufnahmeserien direkt an der Kamera durch. Der Vorschub erfolgt manuell anhand der Skala am Feintrieb des DMLS.
Alle Mikroaufnahmen sind mit Zerene Stacker V1.04 (64bit) gestackt. Die anschließende Nachbereitung beschränkt sich auf die Normalisierung und ein leichtes Nachschärfen nach dem Verkleinern auf die 1024er Auflösung (alles mit XNView in der aktuellen Version). Bei stärker verrauschten Aufnahmen lasse ich aber auch mal Neat Image ran.
Und nun zu den Schnitten
Wie schon so oft weist auch der Querschnitt des Fiederblattes von Ceratozamia robusta im Vergleich zu den bereits besuchten Cycadalesarten einige Überraschungen auf, auch wenn die "Bausteine" bereits von den anderen Arten bekannt sind.
Bilder 8a-h: Übersicht des Fiederblattquerschnitts in der Mitte um am arttypisch umgebogenen Blattrand, Bilder 8a-d vom ungefärbten, frischen Schnitt, Bilder 8e-h vom gefärbten Schnitt, jede zweite Aufnahme mit Maßstab und Beschriftung. Alle Aufnahmen gestapelt
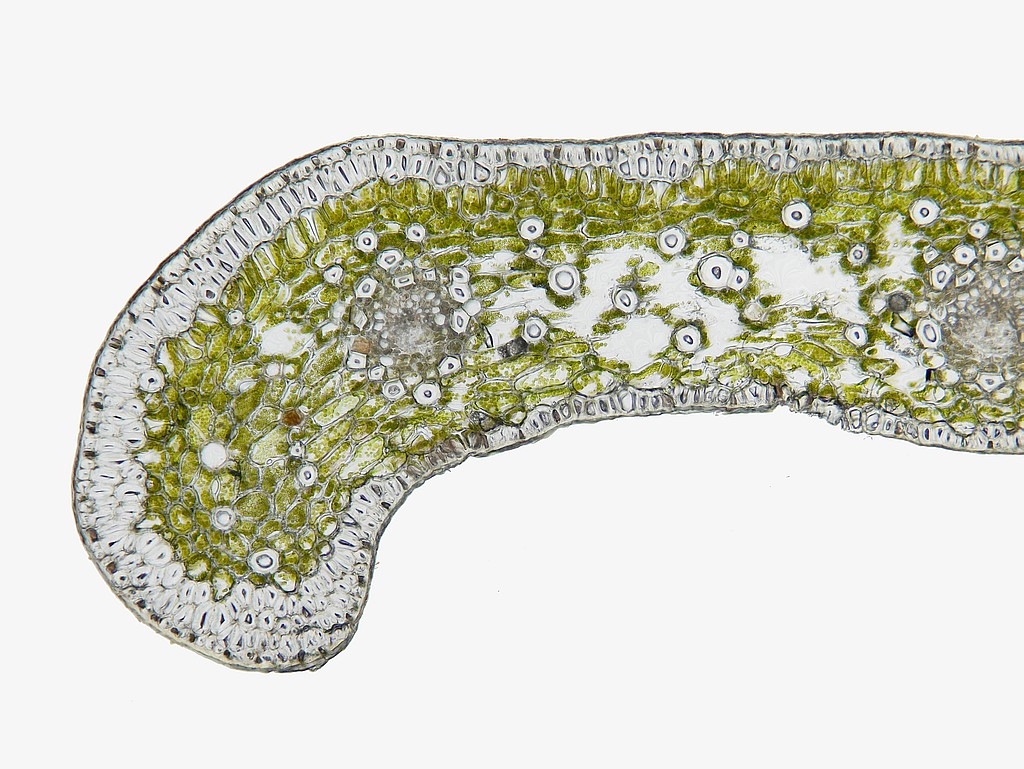

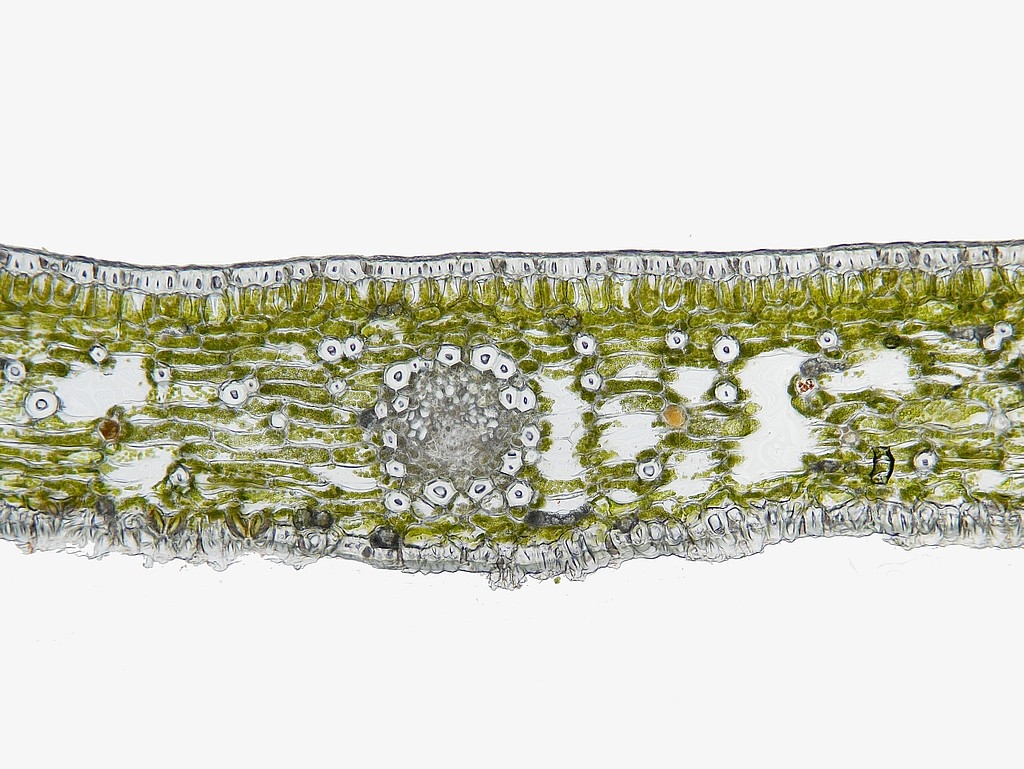
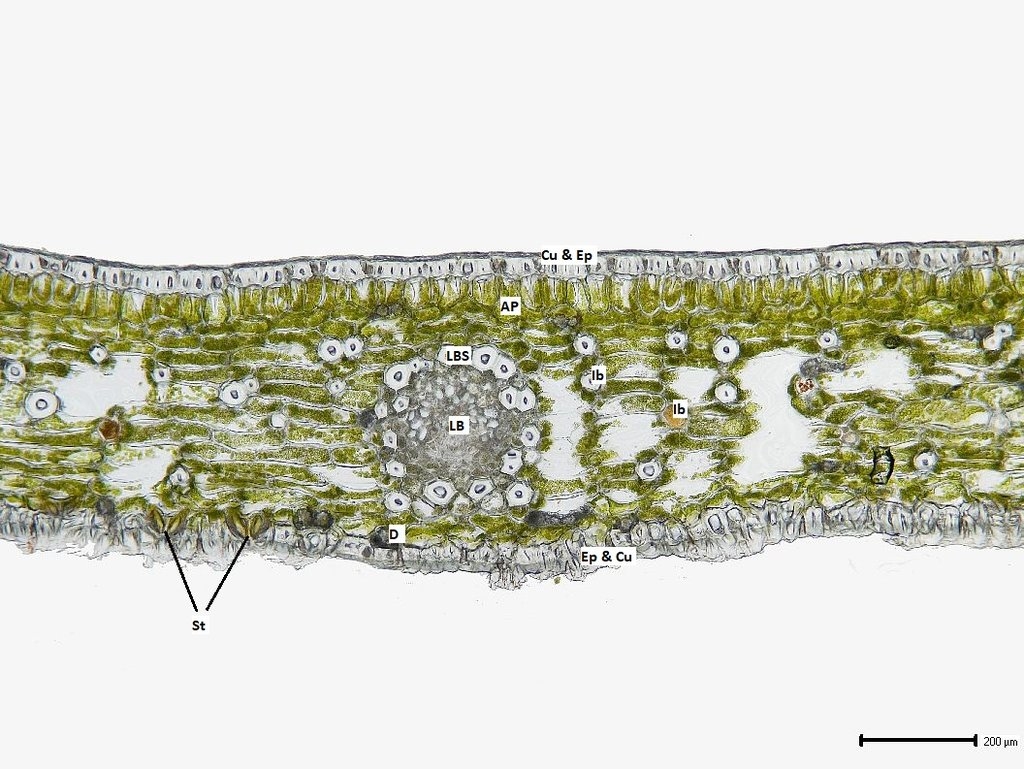

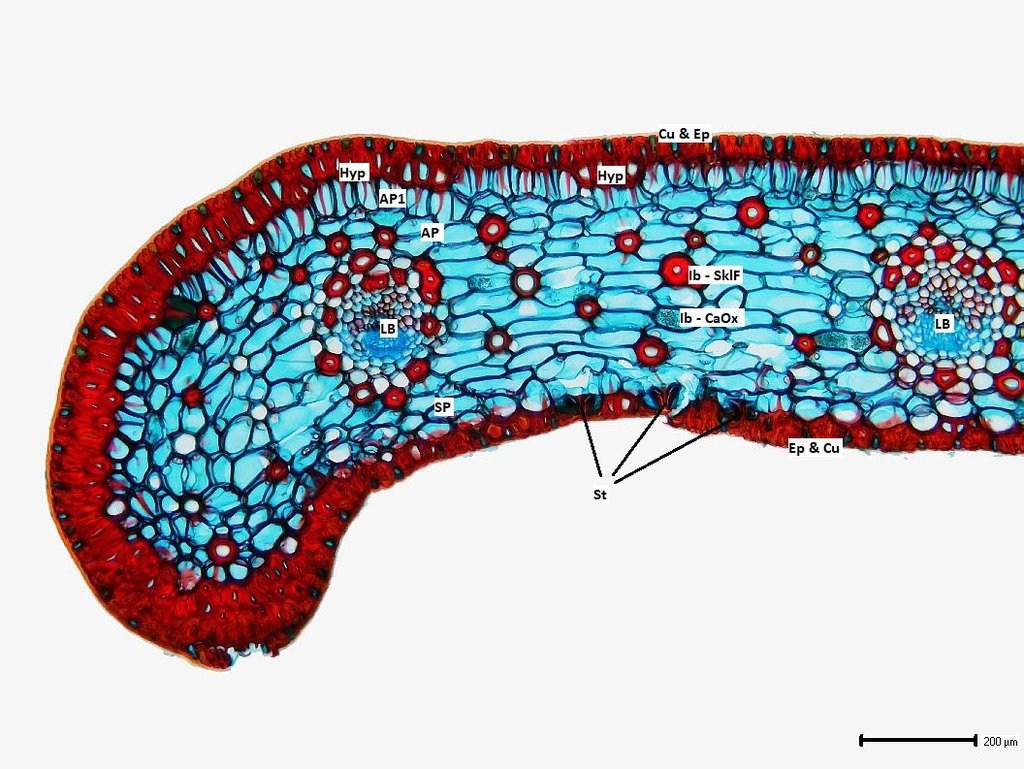

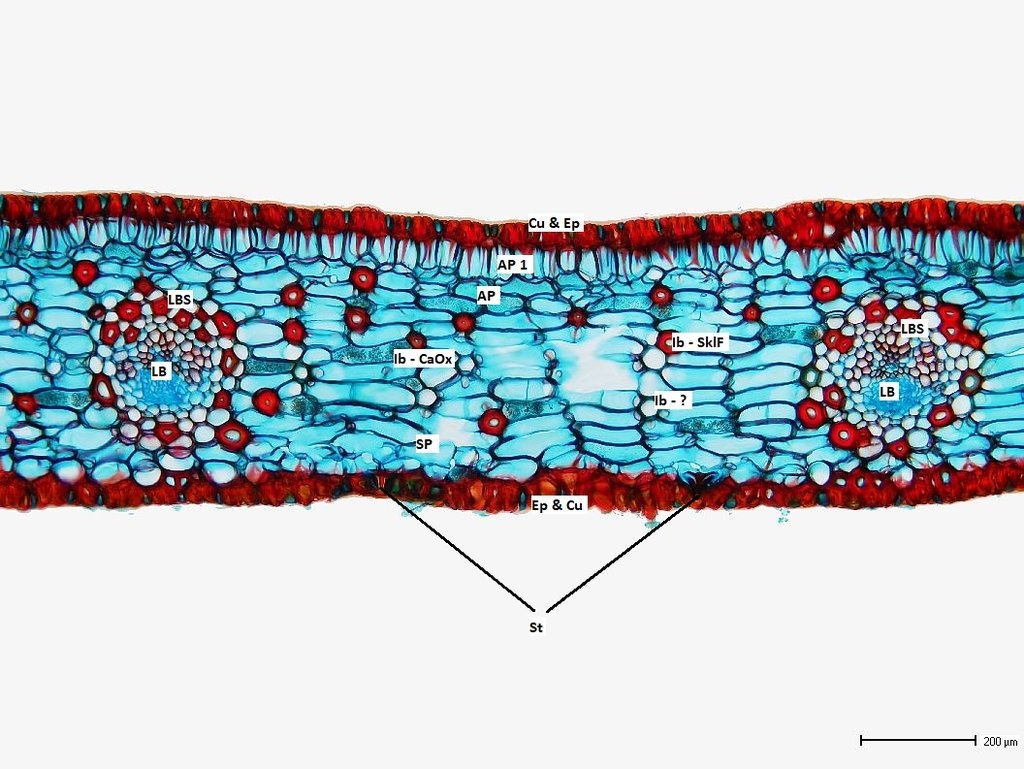
Wir erkennen bereits in der Übersicht den typischen, parallelnervigen Aufbau der Blätter der Cycadaceae. Der umgebogene Rand trägt eine stark ausgeprägte Hypodermis, die teils noch intermittierend vorhanden ist, zur Blattmitte hin aber ausläuft. Darunter liegt eine Zelllage des Assimilationsparenchyms, die sich durch ihre massiven Zellwandverstärkungen von den folgenden Zellagen abhebt. So etwas haben wir auch bei Cycas revoluta schon in noch kräftigerer Ausprägung gesehen (https://www.mikroskopie-forum.de/index.php?topic=4876.0). Zwischen dem Assimilationsparenchym und dem Schwammparenchym des bifazialen Fiederblattes findet sich kein Transfussionsgewebe (TTr). Dessen Auftreten ist bei C. robusta auf das Innere der Leitbündelscheide beschränkt, wie wir in den folgenden Detailaufnahmen noch sehen werden.
Im Mesophyll finden sich drei Arten von Idioblasten: einzelne sklerenchymatische Faserzellen (SklF), einige Zellen mit Calciumoxalat-Drusen (teils zwei in einer Zelle oder als Grus, eventuell durch den Schnitt zerstört) sowie wenige bräunlich angefärbte Zellen, die nur in den frischen Schnitten auffallen und kugelförmig oder in Längsrichtung gestreckt zu sein scheinen. Stomata finden wir in Nestern nur an der Unterseite des Blattes.
Die geschlossen kollateralen Leitbündel liegen in Leitbündelscheiden, die aus parenchymatischen und Faserzellen zusammengesetzt sind. Sie sind von Transfusionstracheiden umgeben.
Faserstränge kommen bei vielen der von mir betrachteten Arten vor (Dioon, Encephalartos), Sekretgänge wie bei den beiden genannten Arten finden sich bei C. robusta jedoch nicht, was er mit der Gattung Cycas gemein hat.
Schauen wir uns nun die einzelnen Merkmale etwas genauer an und beginnen mit zwei aufnahmen im Polarisationskontrast:
Bilder 9a,b: Querschnitte im Polarisationskontrast, beide Aufnahmen gestapelt

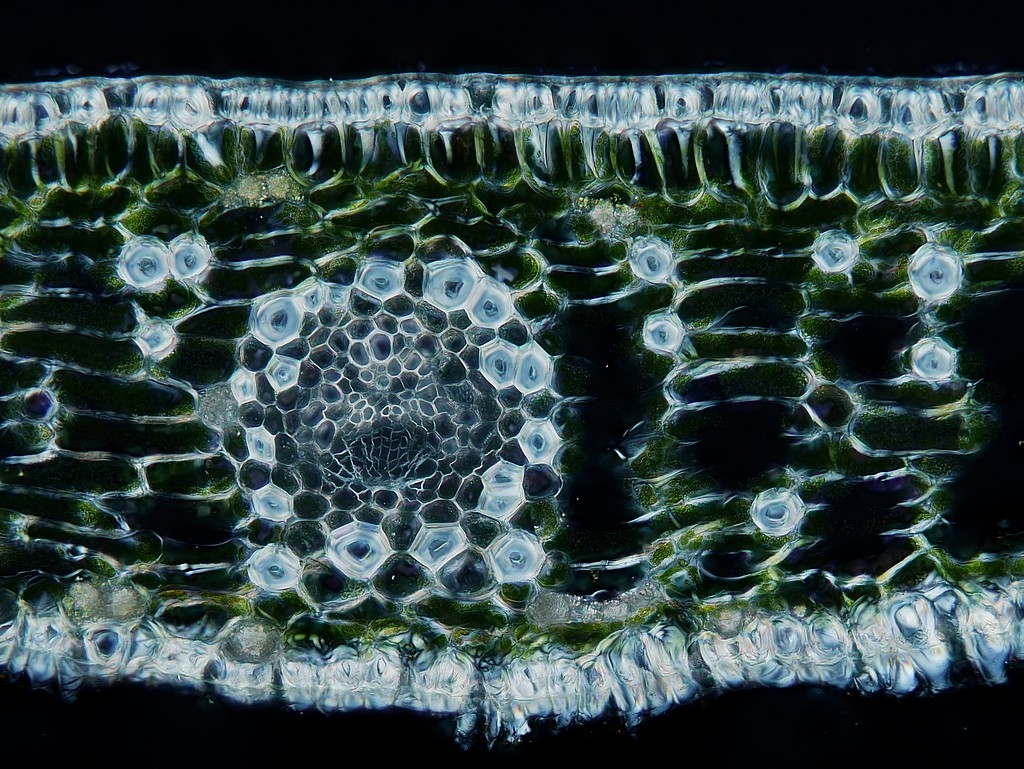
Wie man hier schön sehen kann, sind die Wände aller Zellen im Blattquerschnitt doppelbrechend, was auf die Einlagerung von Zellulosefasern hin weist. Dies gilt selbst für die Zellen des Phloems, die sonst im polarisierten licht nicht in Erscheinung treten. Ebenfalls deutlich zu sehen sind die Drusen in den Zellen am unteren Rand von Bild 9b auf beiden Seiten des Leitbündels.
Weiter geht es mit den Leitbündeln:
Bilder 10a-h: Leitbündel des Fiederblattquerschnitts im umliegenden Gewebe und im Detail, Bilder 10a-d vom ungefärbten, frischen Schnitt, Bilder 10e-h vom gefärbten Schnitt, jede zweite Aufnahme mit Maßstab und Beschriftung. Alle Aufnahmen gestapelt





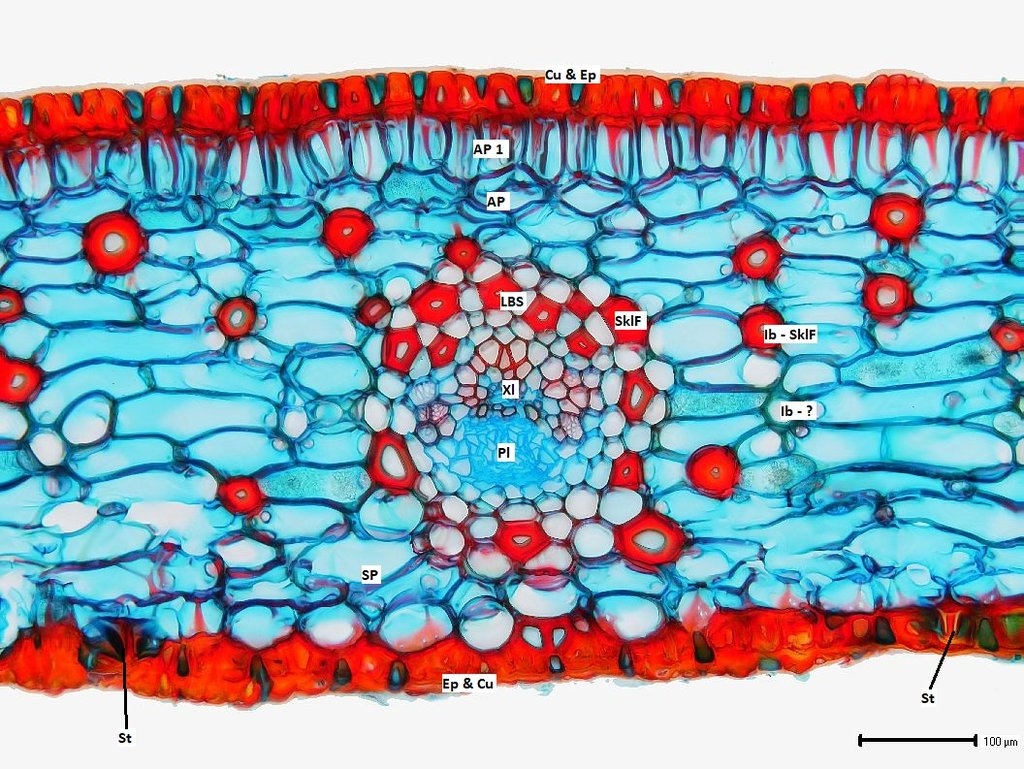


Wir finden die schon oben angesprochene Struktur: ein geschlossen kollaterales Leitbündel mit relativ kleinem Xylem, das vermutlich von dem darum liegenden Transfusionstracheiden kompensiert wird. Drumherum eine Leitbündelscheide aus parenchymatischen Zellen und eingelagerten Faserzellen (SklF). Vereinzelt sind auch Drusen zu sehen.
Werfen wir nun ein Blick auf die Epidermis:
Bilder 11a-f: Epidermis mit sklerenchymatischen und parenchymatischen Zellen, Bilder 11b,d&f mit Beschriftung, alle Aufnahmen gestapelt
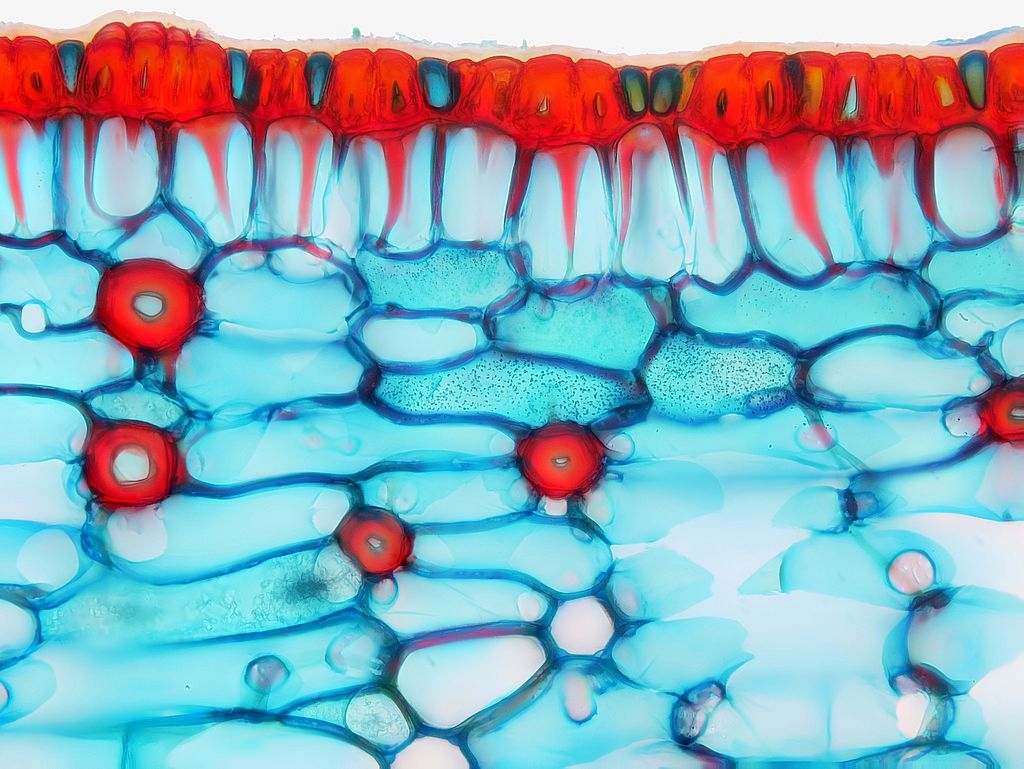

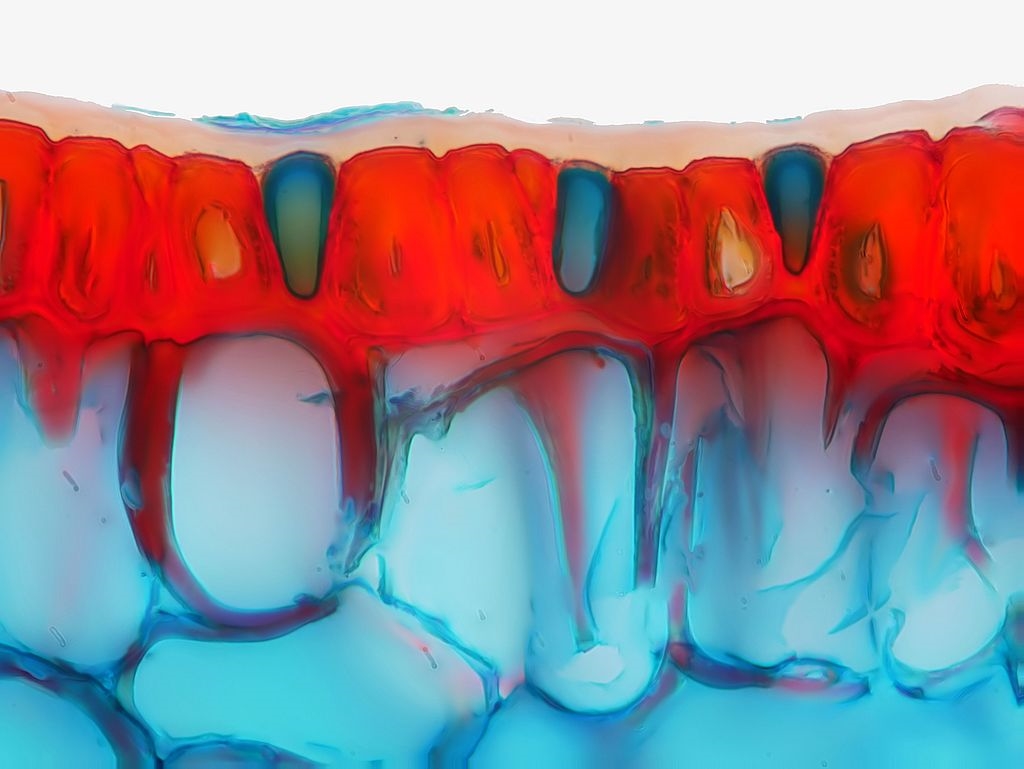
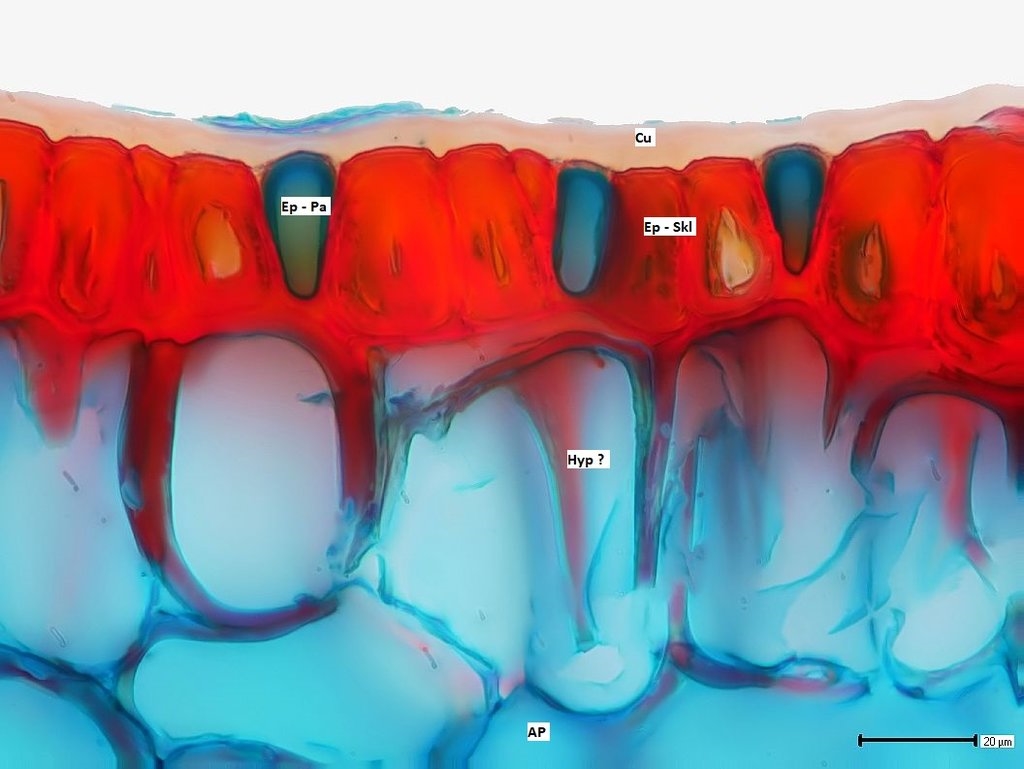


Die Epidermis auf der Blattoberseite ist mit einer dicken Cuticula bedeckt. Am eingerollten Blattrand finden wir eine sklerifizierte, teils zweilagige Hypodermis, die das Blatt mechanisch stabilisiert (11e,f).
Zur Blattmitte hin sind die sklerifizierten Zellen der Epidermis immer wieder von einzeln oder paarweise stehenden parenchymatischen Zellen unterbrochen. Wozu die wohl gut sein mögen?
Bild 12a,b: Eine Doppeldruse ..., Bild 12b mit Beschriftung, beide Aufnahmen gestapelt
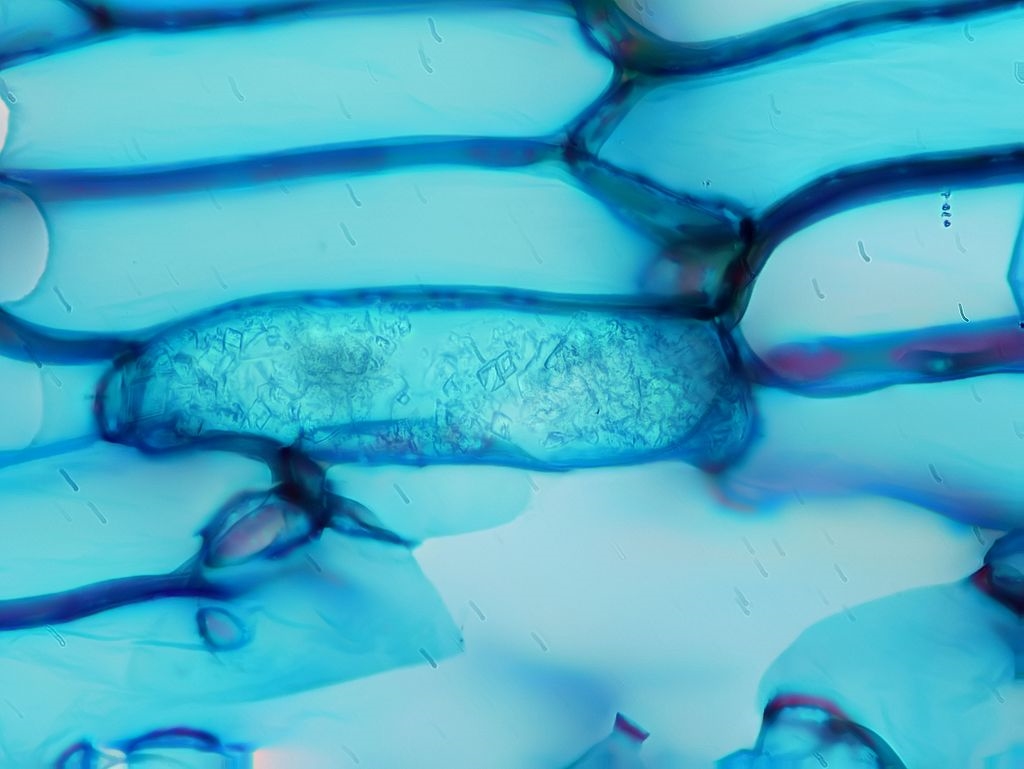
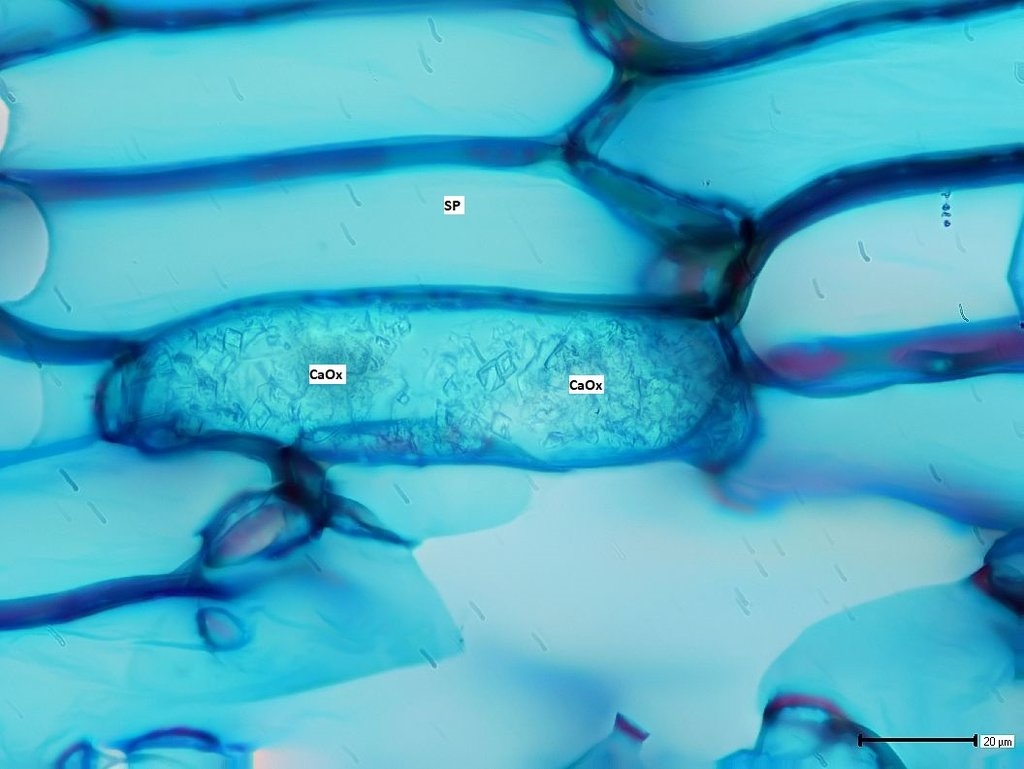
Die in anderen Idioblasten erhaltenen Drusen lassen den Schluss zu, dass in der hier gezeigten Zelle zwei Drusen vorhanden waren, die durch den Schnitt in teils schön rhomboedrisch ausgebildete Einzelkristalle zerstört wurden.
Zum guter Letzt schauen wir noch einmal nach den Stomata:
Bilder 13a-d: Stomata, Bilder 13a&b vom frischen, ungefärbten Schnitt, Bilder 13b&d mit Beschriftung, alle Aufnahmen gestapelt
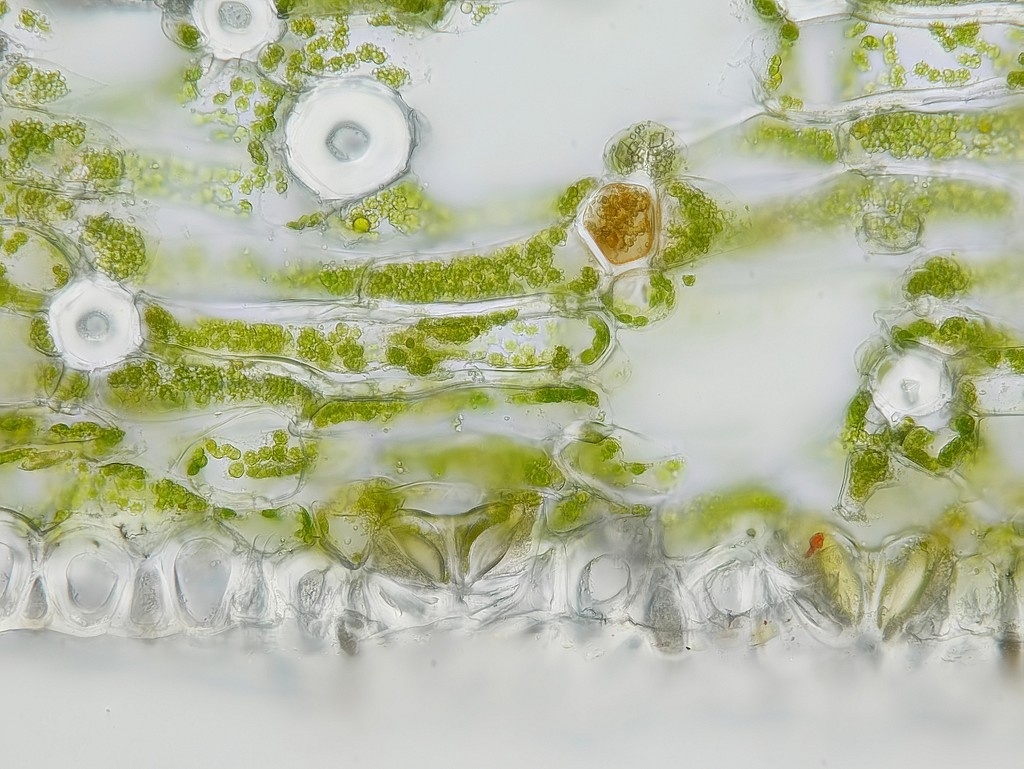

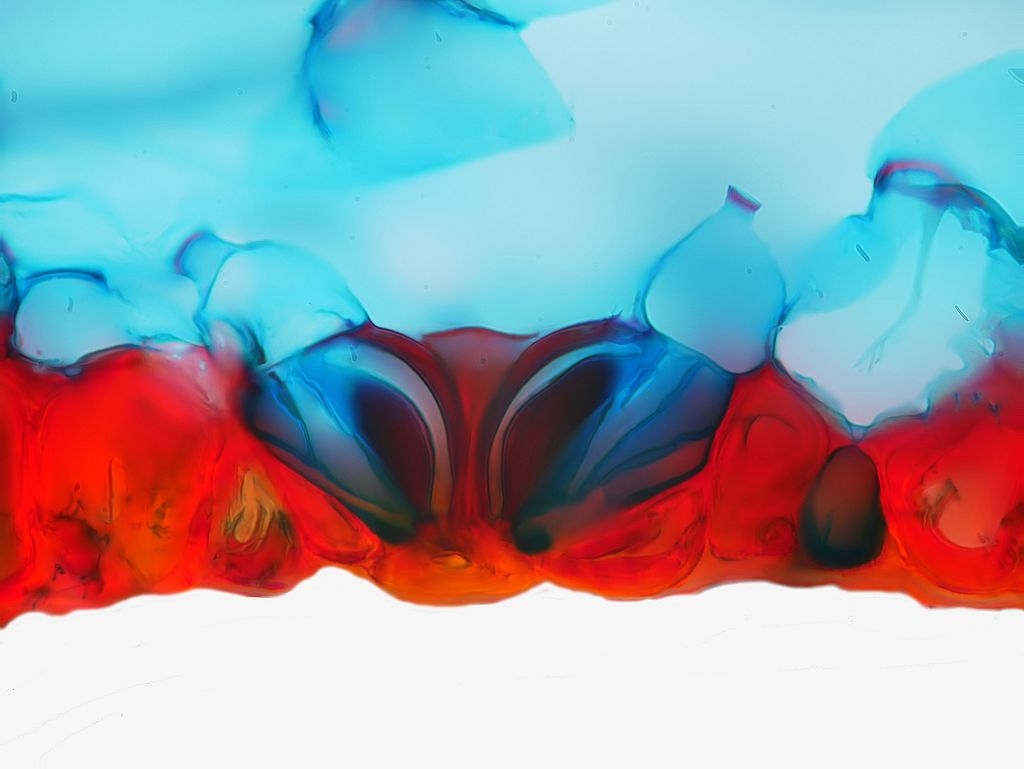
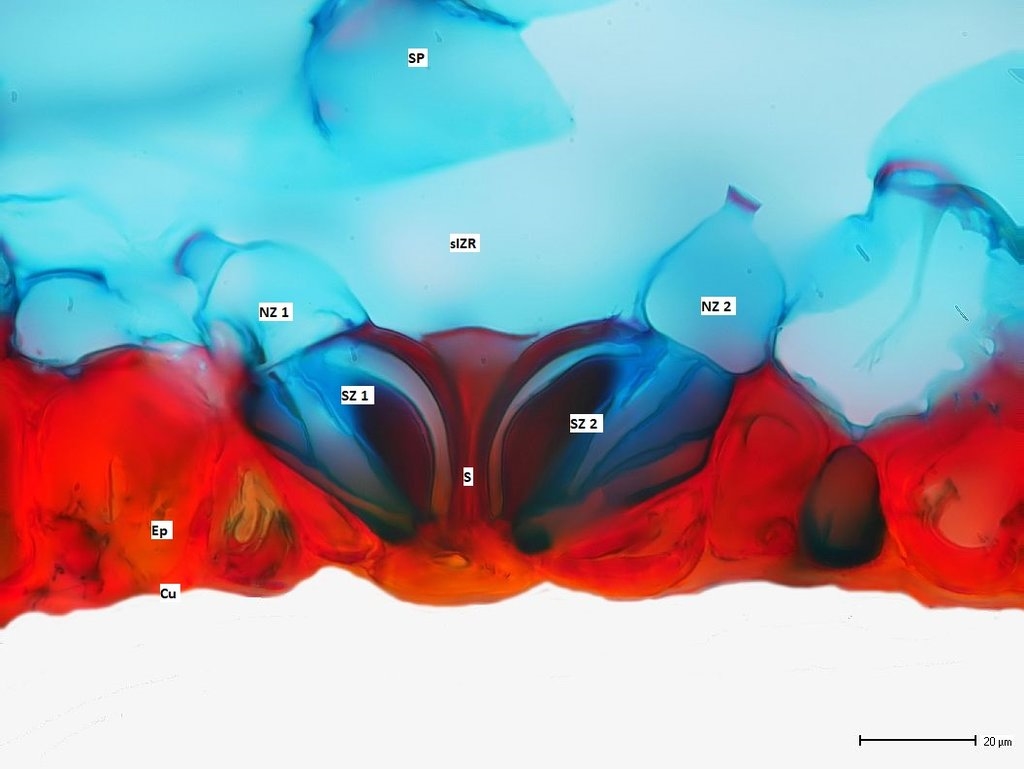
Die Stomata liegen ohne nennenswerten Hof vor recht kleinen Interzellularräumen. Da C. robusta feuchte Habitate bevorzugt, finden wir hier keinerlei Verdunstungsschutz, der in der bevorzugten Umgebung die Wasserverdunstung und damit den Stoffwechsel eher behindern würde. Bei den frischen Schnitten 13a&b ist noch einmal einer der bräunlichen Idioblasten (Ib- ?) zu sehen. Welche Aufgabe der wohl haben mag?
Vielen Dank fürs Lesen, Hinweise und Kritik sind wie immer willkommen.
Herzliche Grüße
Jörg
wo gefunden? Im seit Juni des vergangenen Jahres geöffneten neuen Gewächshaus des Botanischen Gartens Bonn, das im Mittelbeet auch die einzige Sansevieria sambiranensis (jetzt Dracaena sambiranensis) in einem deutschen Botanischen Garten beherbergt. Die Pflanze ist umgeben von einigen schönen Palmfarnen und ich hatte die Tage die Chance, von einem Gärtner ein abgeknicktes Fiederblatt von Ceratozamia robusta zu erhalten.
Ceratozamia ist mit 28 hauptsächlich in den Gebirgszügen Mittelamerikas vorkommenden Arten eine eher kleine Gattung in der Ordnung der Cycadales und die Probe erlaubt mir den Blick auf die Blattanatomie einer weiteren Gattung.
Bild 1: Kladogramm der Ordnung Cycadales mit den bereits von mir beprobten Gattungen

Einen Überblick über meine Beiträge zu den Cycadales findet Ihr hier zu Beginn des Artikels: https://www.mikroskopie-forum.de/index.php?topic=29879.0
Nach nun fast drei Jahren also wieder einmal ein neuer Palmfarn!
Wie immer zunächst etwas zur Pflanze selbst
Ceratozamia robusta ist - obwohl die größte Art der Gattung - ein mittelgroßer Palmfarn, dessen Vorkommen sich von Belize über Guatemala bis nach Mexiko (Oaxaca, Veracruz und ggf. Chiapas) erstreckt. Er findet sein Habitat im Unterholz feuchter, sumpfiger Regenwälder. Die Erstbeschreibung erfolgte 1847 anhand von im Europa kultivierter Pflanzen mit nicht näher bestimmtem Ursprung in Mexiko. Daher wurde 1986 ein Neotyp anhand von Proben verschiedener Pflanze aus Chiapas festgelegt.
Bild 2: Die Pflanze im Botanischen Garten Bonn mit 7 Blättern

Der Oberirdischer Stamm von Ceratozamia robusta erreicht eine Höhe von bis zu 2 m mit einem Durchmesser von ca. 30 cm. Der Stamm ist gelegentlich an der Basis verzweigt. Wie bei den Cycadales üblich ist er von den Blattbasen abgestorbener Blätter bedeckt.
Bild 3: Stamm der bonner Pflanze

Der kleine, kugelige Stamm weist auf ein junges Exemplar hin. An der rechten Seite ein junger Wedel von einem Nebenstamm - ein Hinweis auf die vegetative Vermehrung der Pflanze
Die junge Blätter sind blassgrün und unbehaart. Die Pflanze trägt 8 bis 30 ausgewachsene Blätter, die oft in einer dichten Krone angeordnet sind. Jedes Blatt ist 1,5 bis 3 Meter lang, dunkelgrün und ebenfalls unbehaart. Die einzelnen Blätter oder Wedel haben eine grade bis leicht gebogene Form. Der an der Basis wollig behaarte Blattstiel ist 20 bis 60 cm lang und mit vielen kleinen Stacheln besetzt. Die Rhachis ist gerade bis leicht spiralig gebogen. Pro Blatt finden sich 100 bis 200 lanzettförmige und parallelnervige Fiederblätter mit umgebogenem glatten Rand und spitzem Apex.
Bild 4: Junge Plfanze

Wikipedia, User C. T. Johansson, CC BY-SA 4.0
Der männliche Zapfen ist ca. 30-50 * 10 - 14 cm groß, zylindrisch und steht aufrecht. Die gelblichgrünen Mikrosporophylle tragen 2 kleine, hellbraune Hörnern. Der Fruchtstandsstiel (Peduncle) ist bei einer Dicke von 2,5 cm gut 10 cm lang und auch wollig behaart.
Bild 5: Männliche Zapfen

Wikipedia, User C. T. Johansson, CC BY-SA 4.0
Bild 6: Etwas näher heran erkennt man die beiden Hörnchen an den Enden der Mikrosporophyllen

Crop aus Bild 5, Wikipedia, User C. T. Johansson, CC BY-SA 4.0
Der weiblicher Zapfen erreicht eine Größe von 30 - 50 * 10 - 14 cm, ist ebenfalls zylindrisch geformt und steht aufrecht auf dem etwa 15 cm langen und 2,8 cm dicken Peduncle. Er ist grüngrau gefärbt und die Makrosporophyllen tragen je zwei gut ausgebildeten, kräftigen Hörnern, die farblich nicht abgesetzt sind. Der eiförmige Samen mit weißer Sacrotesta ist etwa 2,5 * 2 cm groß und glatt.
Bild 7: weiblicher Zapfen

Cycads of the World, David L. Jones, S. 121
Beschreibung übertragen aus Cycads of the World von David L. Jones, Smithsonian, zweite Auflage 2002.
Wie immer die Informationen zur Präparation
Probenahme im Botanischen Garten Bonn: ich habe von einem Gärtner ein abgeknicktes Fiederblatt erhalten.
Geschnitten habe ich auf dem Tempelchen (Zylindermikrotom im Halter als Tischmikrotom) mit Leica Einmalklingen 818 im SHK Halter. Das Blatt ist sehr zäh und ließ sich in Möhreneinbettung nicht ganz so gut schneiden (Schnittdicke ca. 50µm).
Anschließend erfolgte die Schnittfixierung in AFE für ca. 14 Stunden. Nach stufenweiser Überführung in Aqua dest stand eine rund dreiminütige Behandlung mit Eau de Javel (DM, Reinigungsprodukt in der Literflasche für kleines Geld mit 2,6g NaClo auf 100 ml) an. Danach habe ich wieder sehr gründlich mit Aqua dest. gespült, bis kein Chlorgeruch mehr erkennbar war. Den Abschluss der Vorbereitungen bildete die Bleiche mit Chloralhydrat (160g auf 100 ml Aqua dest.) für ca. 12 Stunden. Nach einem weiteren sehr gründlichen "Spülgang" waren die schnitte dann bereit für die Färbung.
Gefärbt habe ich nach Überführen in Aqua dest. mit W3Asim I nach Rolf-Dieter Müller für ca. 8 Minuten mit einmaligen Erwärmen bis kurz vor den Siedepunkt.
Eingedeckt wurden die Schnitte nach gründlichem Entwässern mit reinem Isopropanol wie immer in Euparal.
Kurz zur verwendeten Technik
Die Aufnahmen sind auf dem Leica DMLS mit den PlanApos 10x, 20x, 40x und 100x (öl) entstanden. Die Kamera ist eine Panasonic GX7, die am Trinotubus des Mikroskops ohne Zwischenoptik direkt adaptiert ist. Die Steuerung der Kamera erfolgt durch einen elektronischen Fernauslöser. Die notwendigen Einstellungen zur Verschlusszeit und den Weißabgleich führe ich vor den Aufnahmeserien direkt an der Kamera durch. Der Vorschub erfolgt manuell anhand der Skala am Feintrieb des DMLS.
Alle Mikroaufnahmen sind mit Zerene Stacker V1.04 (64bit) gestackt. Die anschließende Nachbereitung beschränkt sich auf die Normalisierung und ein leichtes Nachschärfen nach dem Verkleinern auf die 1024er Auflösung (alles mit XNView in der aktuellen Version). Bei stärker verrauschten Aufnahmen lasse ich aber auch mal Neat Image ran.
Und nun zu den Schnitten
Wie schon so oft weist auch der Querschnitt des Fiederblattes von Ceratozamia robusta im Vergleich zu den bereits besuchten Cycadalesarten einige Überraschungen auf, auch wenn die "Bausteine" bereits von den anderen Arten bekannt sind.
Bilder 8a-h: Übersicht des Fiederblattquerschnitts in der Mitte um am arttypisch umgebogenen Blattrand, Bilder 8a-d vom ungefärbten, frischen Schnitt, Bilder 8e-h vom gefärbten Schnitt, jede zweite Aufnahme mit Maßstab und Beschriftung. Alle Aufnahmen gestapelt








Wir erkennen bereits in der Übersicht den typischen, parallelnervigen Aufbau der Blätter der Cycadaceae. Der umgebogene Rand trägt eine stark ausgeprägte Hypodermis, die teils noch intermittierend vorhanden ist, zur Blattmitte hin aber ausläuft. Darunter liegt eine Zelllage des Assimilationsparenchyms, die sich durch ihre massiven Zellwandverstärkungen von den folgenden Zellagen abhebt. So etwas haben wir auch bei Cycas revoluta schon in noch kräftigerer Ausprägung gesehen (https://www.mikroskopie-forum.de/index.php?topic=4876.0). Zwischen dem Assimilationsparenchym und dem Schwammparenchym des bifazialen Fiederblattes findet sich kein Transfussionsgewebe (TTr). Dessen Auftreten ist bei C. robusta auf das Innere der Leitbündelscheide beschränkt, wie wir in den folgenden Detailaufnahmen noch sehen werden.
Im Mesophyll finden sich drei Arten von Idioblasten: einzelne sklerenchymatische Faserzellen (SklF), einige Zellen mit Calciumoxalat-Drusen (teils zwei in einer Zelle oder als Grus, eventuell durch den Schnitt zerstört) sowie wenige bräunlich angefärbte Zellen, die nur in den frischen Schnitten auffallen und kugelförmig oder in Längsrichtung gestreckt zu sein scheinen. Stomata finden wir in Nestern nur an der Unterseite des Blattes.
Die geschlossen kollateralen Leitbündel liegen in Leitbündelscheiden, die aus parenchymatischen und Faserzellen zusammengesetzt sind. Sie sind von Transfusionstracheiden umgeben.
Faserstränge kommen bei vielen der von mir betrachteten Arten vor (Dioon, Encephalartos), Sekretgänge wie bei den beiden genannten Arten finden sich bei C. robusta jedoch nicht, was er mit der Gattung Cycas gemein hat.
Schauen wir uns nun die einzelnen Merkmale etwas genauer an und beginnen mit zwei aufnahmen im Polarisationskontrast:
Bilder 9a,b: Querschnitte im Polarisationskontrast, beide Aufnahmen gestapelt


Wie man hier schön sehen kann, sind die Wände aller Zellen im Blattquerschnitt doppelbrechend, was auf die Einlagerung von Zellulosefasern hin weist. Dies gilt selbst für die Zellen des Phloems, die sonst im polarisierten licht nicht in Erscheinung treten. Ebenfalls deutlich zu sehen sind die Drusen in den Zellen am unteren Rand von Bild 9b auf beiden Seiten des Leitbündels.
Weiter geht es mit den Leitbündeln:
Bilder 10a-h: Leitbündel des Fiederblattquerschnitts im umliegenden Gewebe und im Detail, Bilder 10a-d vom ungefärbten, frischen Schnitt, Bilder 10e-h vom gefärbten Schnitt, jede zweite Aufnahme mit Maßstab und Beschriftung. Alle Aufnahmen gestapelt








Wir finden die schon oben angesprochene Struktur: ein geschlossen kollaterales Leitbündel mit relativ kleinem Xylem, das vermutlich von dem darum liegenden Transfusionstracheiden kompensiert wird. Drumherum eine Leitbündelscheide aus parenchymatischen Zellen und eingelagerten Faserzellen (SklF). Vereinzelt sind auch Drusen zu sehen.
Werfen wir nun ein Blick auf die Epidermis:
Bilder 11a-f: Epidermis mit sklerenchymatischen und parenchymatischen Zellen, Bilder 11b,d&f mit Beschriftung, alle Aufnahmen gestapelt






Die Epidermis auf der Blattoberseite ist mit einer dicken Cuticula bedeckt. Am eingerollten Blattrand finden wir eine sklerifizierte, teils zweilagige Hypodermis, die das Blatt mechanisch stabilisiert (11e,f).
Zur Blattmitte hin sind die sklerifizierten Zellen der Epidermis immer wieder von einzeln oder paarweise stehenden parenchymatischen Zellen unterbrochen. Wozu die wohl gut sein mögen?
Bild 12a,b: Eine Doppeldruse ..., Bild 12b mit Beschriftung, beide Aufnahmen gestapelt


Die in anderen Idioblasten erhaltenen Drusen lassen den Schluss zu, dass in der hier gezeigten Zelle zwei Drusen vorhanden waren, die durch den Schnitt in teils schön rhomboedrisch ausgebildete Einzelkristalle zerstört wurden.
Zum guter Letzt schauen wir noch einmal nach den Stomata:
Bilder 13a-d: Stomata, Bilder 13a&b vom frischen, ungefärbten Schnitt, Bilder 13b&d mit Beschriftung, alle Aufnahmen gestapelt




Die Stomata liegen ohne nennenswerten Hof vor recht kleinen Interzellularräumen. Da C. robusta feuchte Habitate bevorzugt, finden wir hier keinerlei Verdunstungsschutz, der in der bevorzugten Umgebung die Wasserverdunstung und damit den Stoffwechsel eher behindern würde. Bei den frischen Schnitten 13a&b ist noch einmal einer der bräunlichen Idioblasten (Ib- ?) zu sehen. Welche Aufgabe der wohl haben mag?
Vielen Dank fürs Lesen, Hinweise und Kritik sind wie immer willkommen.
Herzliche Grüße
Jörg
Titel: Re: Botanik: Ein seltener Fund - Ceratozamia robusta *
Beitrag von: Hans-Jürgen Koch in März 10, 2019, 10:24:36 VORMITTAG
Beitrag von: Hans-Jürgen Koch in März 10, 2019, 10:24:36 VORMITTAG
Lieber Jörg,
es hat schon Vorteile, wenn man einen netten Gärtner kennt.
Super Beitrag.
Warum hast du Eau de Javel und Chloralhydrat zusammen eingesetzt ?
Gruß
Hans-Jürgen
es hat schon Vorteile, wenn man einen netten Gärtner kennt.
Super Beitrag.
Warum hast du Eau de Javel und Chloralhydrat zusammen eingesetzt ?
Gruß
Hans-Jürgen
Titel: Re: Botanik: Ein seltener Fund - Ceratozamia robusta *
Beitrag von: Fahrenheit in März 10, 2019, 16:12:23 NACHMITTAGS
Beitrag von: Fahrenheit in März 10, 2019, 16:12:23 NACHMITTAGS
Lieber Hans-Jürgen,
vielen Dank für Dein Lob, das mich wie immer sehr freut!
Das Eau de Javel hat Rolf-Dieter Müller die Tage bei DM in der Literflasche entdeckt. Als "Chemikalie" kann man es als Privatperson quasi nicht beziehen. Da ist ja so'n furchtbar gefährliches Höllenzeugs drin ... ;D
Bisher hatte ich Klorix (1:4 verdünnt) verwendet, es basiert auf Natriumhypochlorid, Eau de Javel basiert auf Kaliumhypochlorid (https://de.wikipedia.org/wiki/Javelwasser).
Uups!
Eben nehme ich die Flasche zur Hand: das Eau de Javel vom DM läuft auch mit Natriumhypochlorid ... interessant, hatte ich noch garnicht gesehen. Da kann man als Nicht-Chemicus auch weiter Klorix nehmen, da lässt sich die Konzentration selbst bestimmen. :(
Also, warum Eua de Javel / Klorix: das Hypochlorid zerstört die Zellinhalte, der Schnitt ist nachher fein geputzt. Nur ganz hartnäckige ätherische Öle überleben. Aber es werden auch die Mittellamellen angegriffen: wenn man nicht aufpasst zerfallen die Schnitte. Damit ist die Einwirkzeit begrenzt und oft färben sich die Schnitte - vermutlich wegen der Abbauprodukte - erst einmal bräunlich.
Das Chloralhydrat hingegen greift die Strukturen nicht so sehr an, es bleicht nur. In Kombination mit beiden bekommt man sauber geputzte Schnitte fast ohne Eigenfärbung und erhält damit schön brillante Farben aus den Färbungen. Am auffälligsten ist das nach meiner Erfahrung bei Gymnospermen. Am besten in der Kombination mit Dujardin Grün, zu dem ich die benötigte Acliangrün-Lösung zur Zeit leider nicht zur Hand habe.
Herzliche Grüße
Jörg
vielen Dank für Dein Lob, das mich wie immer sehr freut!
Das Eau de Javel hat Rolf-Dieter Müller die Tage bei DM in der Literflasche entdeckt. Als "Chemikalie" kann man es als Privatperson quasi nicht beziehen. Da ist ja so'n furchtbar gefährliches Höllenzeugs drin ... ;D
Bisher hatte ich Klorix (1:4 verdünnt) verwendet, es basiert auf Natriumhypochlorid, Eau de Javel basiert auf Kaliumhypochlorid (https://de.wikipedia.org/wiki/Javelwasser).
Uups!
Eben nehme ich die Flasche zur Hand: das Eau de Javel vom DM läuft auch mit Natriumhypochlorid ... interessant, hatte ich noch garnicht gesehen. Da kann man als Nicht-Chemicus auch weiter Klorix nehmen, da lässt sich die Konzentration selbst bestimmen. :(
Also, warum Eua de Javel / Klorix: das Hypochlorid zerstört die Zellinhalte, der Schnitt ist nachher fein geputzt. Nur ganz hartnäckige ätherische Öle überleben. Aber es werden auch die Mittellamellen angegriffen: wenn man nicht aufpasst zerfallen die Schnitte. Damit ist die Einwirkzeit begrenzt und oft färben sich die Schnitte - vermutlich wegen der Abbauprodukte - erst einmal bräunlich.
Das Chloralhydrat hingegen greift die Strukturen nicht so sehr an, es bleicht nur. In Kombination mit beiden bekommt man sauber geputzte Schnitte fast ohne Eigenfärbung und erhält damit schön brillante Farben aus den Färbungen. Am auffälligsten ist das nach meiner Erfahrung bei Gymnospermen. Am besten in der Kombination mit Dujardin Grün, zu dem ich die benötigte Acliangrün-Lösung zur Zeit leider nicht zur Hand habe.
Herzliche Grüße
Jörg
Titel: Re: Botanik: Ein seltener Fund - Ceratozamia robusta *
Beitrag von: Frank Fox in März 10, 2019, 17:14:02 NACHMITTAGS
Beitrag von: Frank Fox in März 10, 2019, 17:14:02 NACHMITTAGS
Lieber Jörg,
das sind fantastische Schnitte.
:)
Herzliche Grüße
Frank
das sind fantastische Schnitte.
:)
Herzliche Grüße
Frank
Titel: Re: Botanik: Ein seltener Fund - Ceratozamia robusta *
Beitrag von: Wutsdorff Peter in März 11, 2019, 10:58:58 VORMITTAG
Beitrag von: Wutsdorff Peter in März 11, 2019, 10:58:58 VORMITTAG
Hallo Jörg,
ich bin sprachlos und voller Bewunderung Deiner Bilder und Deines fundierten Wissens.
SSSUUUUPPEEEER!!!
Da traue ich mich nicht, meine eigenen Schnitte zu zeigen.
Jetzt noch eine dumme Frage: Proben und Schnitte beware ich in AFE auf.
Muß ich dann noch anschleißend den Schnitt in reines Ethanol überführen, oder kann ich gleich in Ethanol 70% überführen? Dann geht es weiter wie üblich.
Damit beim Eindecken in Euparal die Schnitte nicht weglaufen, nachdem ich sie schon vorher auf dem DG mit Eup. mit ein- bis zwei Tr. Eup. eingedeckt habe (ca 6-6 Min antrocknen, Trick von Rainer), verschmiere ich das Eup. auf dem OT auf die größe des DG´s. Da die Schn. auf dem DG schon etwas angetrocknet sind, laufen sie unter dem verschmierten Eup. auf dem OT nicht weg. Beim Tropfen auf dem OT laufen die Schn. nämlch trotzdem weg.
Das funktioniert recht gut.
Gruß Peter
ich bin sprachlos und voller Bewunderung Deiner Bilder und Deines fundierten Wissens.
SSSUUUUPPEEEER!!!
Da traue ich mich nicht, meine eigenen Schnitte zu zeigen.
Jetzt noch eine dumme Frage: Proben und Schnitte beware ich in AFE auf.
Muß ich dann noch anschleißend den Schnitt in reines Ethanol überführen, oder kann ich gleich in Ethanol 70% überführen? Dann geht es weiter wie üblich.
Damit beim Eindecken in Euparal die Schnitte nicht weglaufen, nachdem ich sie schon vorher auf dem DG mit Eup. mit ein- bis zwei Tr. Eup. eingedeckt habe (ca 6-6 Min antrocknen, Trick von Rainer), verschmiere ich das Eup. auf dem OT auf die größe des DG´s. Da die Schn. auf dem DG schon etwas angetrocknet sind, laufen sie unter dem verschmierten Eup. auf dem OT nicht weg. Beim Tropfen auf dem OT laufen die Schn. nämlch trotzdem weg.
Das funktioniert recht gut.
Gruß Peter
Titel: Re: Botanik: Ein seltener Fund - Ceratozamia robusta *
Beitrag von: Fahrenheit in März 11, 2019, 11:56:22 VORMITTAG
Beitrag von: Fahrenheit in März 11, 2019, 11:56:22 VORMITTAG
Lieber Frank, lieber Peter,
auch euch vielen Dank für Euer Lob! Es frut mich sehr, dass Euch der Beitrag gefällt.
@Peter
Zeige ruhig Deine Schnitte, dann könne wir ggf. unterstützen! Meine wahren vor 10 Jahren auch erst mal ziemlich übel und die Kolleginnen und Kollegen im Forum haben mir geholfen, besser zu werden. Dazu kommt natürlich auch immer die Übung.
Hier war die Vorbereitung zur Färbung mit Eau de Javel und Chloralhydrat auch etwas komplexa als beim Standardvorgehen. Belohnt wird das ganze dann durch schön saubere Schnitte.
AFE hat ja ungefähr einen Ethanolgehalt von 70%, der Umweg über reines Ethanol ist also unnötig. Nach dem Fixieren einfach mit Ethanol 70% spülen und dann stufenweise ins Aqua dest. überführen.
Beim Auflegen des Deckglases kann es schon sein, dass der Schnitt ausbüxt. Ich stoppe die Bewegung mit der Rückseite der Pipette (einfach sanft auf die Seite des Deckgläschens drücken, zu der der Schnitt abwandert). Wenn ich nicht schnell genug bin, muss ich eben neu eindecken. ;)
Euch beiden herzliche Grüße
Jörg
auch euch vielen Dank für Euer Lob! Es frut mich sehr, dass Euch der Beitrag gefällt.
@Peter
Zeige ruhig Deine Schnitte, dann könne wir ggf. unterstützen! Meine wahren vor 10 Jahren auch erst mal ziemlich übel und die Kolleginnen und Kollegen im Forum haben mir geholfen, besser zu werden. Dazu kommt natürlich auch immer die Übung.
Hier war die Vorbereitung zur Färbung mit Eau de Javel und Chloralhydrat auch etwas komplexa als beim Standardvorgehen. Belohnt wird das ganze dann durch schön saubere Schnitte.
AFE hat ja ungefähr einen Ethanolgehalt von 70%, der Umweg über reines Ethanol ist also unnötig. Nach dem Fixieren einfach mit Ethanol 70% spülen und dann stufenweise ins Aqua dest. überführen.
Beim Auflegen des Deckglases kann es schon sein, dass der Schnitt ausbüxt. Ich stoppe die Bewegung mit der Rückseite der Pipette (einfach sanft auf die Seite des Deckgläschens drücken, zu der der Schnitt abwandert). Wenn ich nicht schnell genug bin, muss ich eben neu eindecken. ;)
Euch beiden herzliche Grüße
Jörg
Titel: Re: Botanik: Ein seltener Fund - Ceratozamia robusta *
Beitrag von: Hugo Halfmann in März 11, 2019, 12:18:51 NACHMITTAGS
Beitrag von: Hugo Halfmann in März 11, 2019, 12:18:51 NACHMITTAGS
Hallo Jörg,
wozu die Behandlung mit Klorix und Chloralhydrat? Macht das die zähen Blätter weicher? Bitte erleuchte mich!
wozu die Behandlung mit Klorix und Chloralhydrat? Macht das die zähen Blätter weicher? Bitte erleuchte mich!
Titel: Re: Botanik: Ein seltener Fund - Ceratozamia robusta *
Beitrag von: Fahrenheit in März 11, 2019, 15:51:26 NACHMITTAGS
Beitrag von: Fahrenheit in März 11, 2019, 15:51:26 NACHMITTAGS
Lieber Hugo,
wie oben in der Antwort an Hans-Jürgen schon dargelegt: Klorix / Eau de Javel putzt die Zellen, greift aber auch die Zellwände an, Chloralhydrat bleicht und ist dabei nicht so aggressive.
Am Ende hast Du saubere Zellen ohne Zellinhalt, die nahezu keine Eigenfärbung mehr haben.
Herzliche Grüße
Jörg
p.s. Der ganze Präparationsablauf ist hier genauer beschrieben:
http://www.mikroskopie-bonn.de/themenseiten/erstellung_pflanzlicher_dauerpraeparate/index.php
wie oben in der Antwort an Hans-Jürgen schon dargelegt: Klorix / Eau de Javel putzt die Zellen, greift aber auch die Zellwände an, Chloralhydrat bleicht und ist dabei nicht so aggressive.
Am Ende hast Du saubere Zellen ohne Zellinhalt, die nahezu keine Eigenfärbung mehr haben.
Herzliche Grüße
Jörg
p.s. Der ganze Präparationsablauf ist hier genauer beschrieben:
http://www.mikroskopie-bonn.de/themenseiten/erstellung_pflanzlicher_dauerpraeparate/index.php